CAR-工程化细胞检测解决方案
基于嵌合抗原受体 (CAR) 的细胞疗法的开发正在彻底改变人类癌症和自身免疫性疾病的治疗。随着这种创新的治疗方式不断改进并变得更加容易获得,更好的试剂正在提高我们检测、识别和充分检测 CAR 表达细胞的能力。凭借不断增长的创新产品组合,CST 正在帮助推进该领域研究人员的工作。
更轻松、更快速地检测 CAR 工程化细胞
科学家在开发和检测 CAR 工程化细胞时面临的最大挑战之一是需要强大、灵敏且有选择性的研究试剂来识别 CAR 工程化细胞。如果您计划在研究中使用免疫检测,那么开发自己的抗独特型抗体来识别 CAR 工程化细胞可能会是一个漫长且耗费资源的过程。
用于检测 CAR 工程化细胞的工作流程解决方案
检测 CAR 工程化细胞的复杂过程有许多阶段。CST 专注于该过程中的一个关键步骤,并开发了一套专门用于 CAR 细胞检测的研究工具。
为了简化您的分析,CST 科学家针对基于 scFv 的 CAR 普遍存在的肽接头序列开发了重组单克隆抗体。通过靶向这些普遍存在的接头序列,您可以消除对所测试的每个 CAR 变体的抗独特型抗体的需求,从而显著减少时间、精力和成本。我们的 CAR Linker抗体对 G4S 或 Whitlow/218 接头具有高度特异性,因此可以检测基于 scFv 的 CAR 表达,而不依赖于 scFv 的特异性。
CAR 检测
- 用于流式细胞术的 G4S Linker 抗体
- 使用 G4S Linker 检测表面表达的基于 scFv 的 CAR,与 scFv 抗原特异性无关
- 在多参数流式检验组合中表现良好
- 用于流式细胞术的 Whitlow/218 Linker 抗体
- 使用 Whitlow/218 Linker 检测表面表达的基于 scFv 的 CAR,与 scFv 抗原特异性无关
- 在多参数流式检验组合中表现良好
- CAR Linker 抗体 F(ab')2 片段偶联物
- 蛋白 L 偶联物
- CAR Linker ELISA 试剂盒
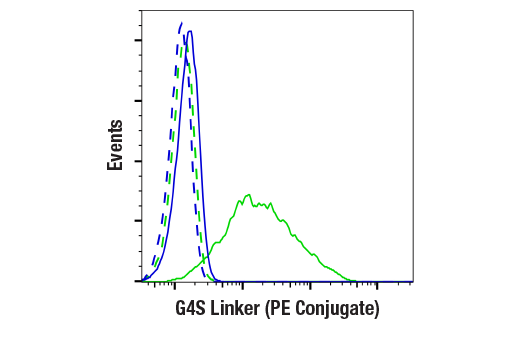
使用 G4S Linker (E7O2V) Rabbit mAb (PE Conjugate)(实线)或浓度匹配的 Rabbit (DA1E) mAb IgG XP® Isotype Control (PE Conjugate) #5742(虚线),对活性 Jurkat 细胞(蓝色,阴性)或经工程化以稳定表达含有 G4S Linker 的基于 scFv 的抗 CD20 CAR 的 Jurkat 细胞(绿色,阳性)进行流式细胞分析。细胞系由匹兹堡大学 Lohmueller 实验室提供。
对照
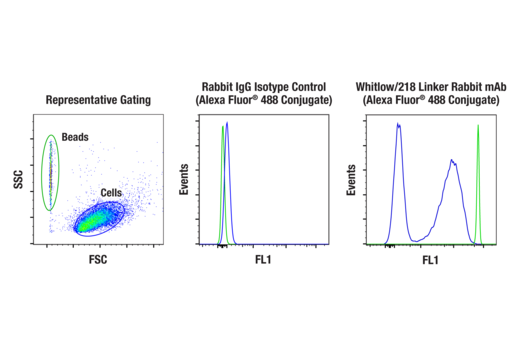
将 Whitlow/218 Linker Posibeads™ 对照添加到含有野生型 Jurkat 细胞和经过工程化以表达含有 Whitlow/218 接头的基于 scFv 的抗 CD19 CAR 的 Jurkat 细胞的混合活细胞群中。然后用 Rabbit (DA1E) mAb IgG XP® Isotype Control (Alexa Fluor® 488 Conjugate) #2975(中图)或 Whitlow/218 Linker (E3U7Q) Rabbit mAb (Alexa Fluor® 488 Conjugate) #55809(右图)对细胞和 Posibeads 对照进行免疫染色。如图所示(左图),细胞和珠子通过前向散射 (FSC) 和侧向散射 (SSC) 进行区分,并且两种免疫染色条件下的细胞 (蓝色) 和 Posibeads 对照 (绿色) 的荧光数据 (FL1) 均显示。CAR 细胞系由匹兹堡大学 Lohmueller 实验室提供。
靶标抗原检测
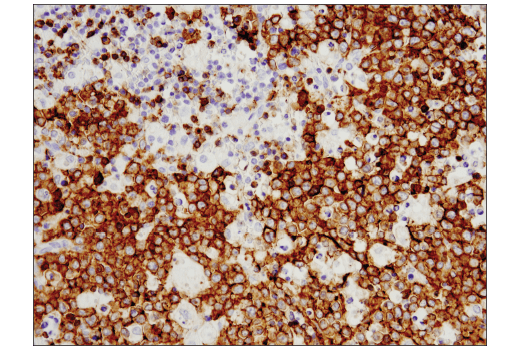
使用 CD19 (Intracellular Domain) (D4V4B) XP® Rabbit mAb #90176 对石蜡包埋的人淋巴瘤组织进行免疫组织化学分析。
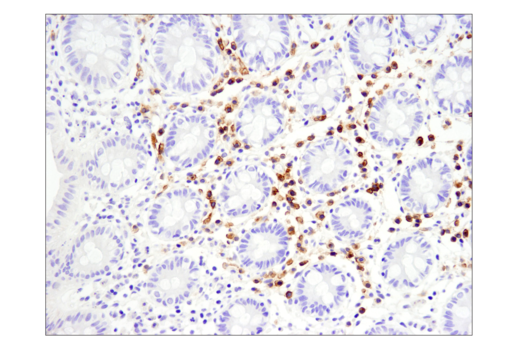
使用 TNFRSF17/BCMA (E6D7B) Rabbit mAb #88183 对石蜡包埋的人正常结肠组织进行免疫组织化学分析。
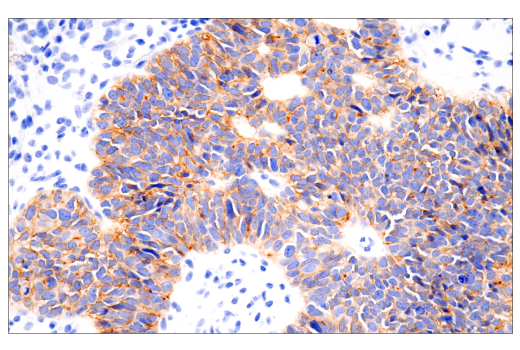
在 Leica BOND Rx 上,使用 Claudin-6 (E7U2O) XP® Rabbit mAb #18932 对石蜡包埋的人卵巢浆液性乳头状癌组织进行免疫组织化学分析。
T 细胞激活
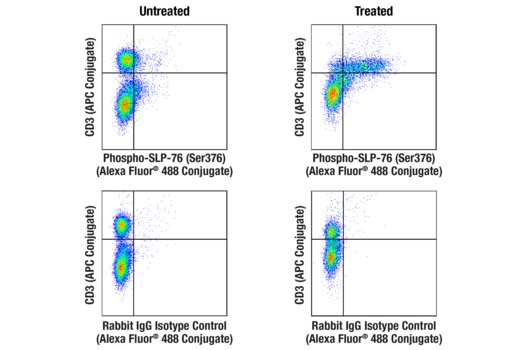
使用 Phospho-SLP-76 (Ser376) (E3G9U) XP® Rabbit mAb (Alexa Fluor® 488 Conjugate) #47876(上行)或浓度匹配的 Rabbit (DA1E) mAb IgG XP® Isotype Control (Alexa Fluor® 488 Conjugate) #2975(下行)和共染色的 CD3 (17A2) Rat mAb (APC Conjugate) #24265,对未经处理(左栏)或经 Rapid-Act T-Cell Activation Kit #86772 (Mouse, Anti-CD3/CD28)(15 分钟;右栏)处理的小鼠脾细胞进行流式细胞分析。
细胞增殖
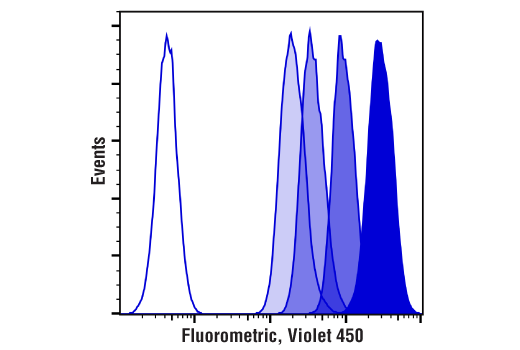
在 4 天(d0-d3)的过程中跟踪 Jurkat 活细胞的细胞分裂。将细胞在第 0 天用 Cell Proliferation Tracer Kit (Fluorometric, Violet 450) #48444 标记,并每天通过流式细胞术分析。每个相继较暗的峰代表一个细胞分裂。未染色的细胞由无阴影峰表示。
细胞毒性分析
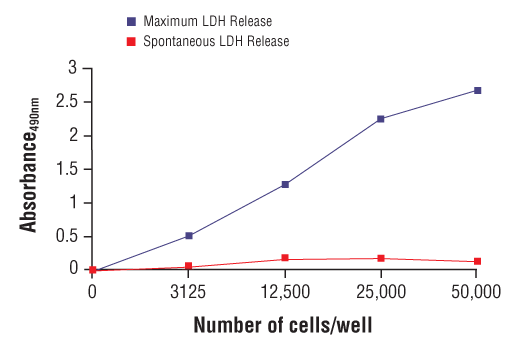
使用含有 10% FBS 的培养基,将 HeLa 细胞以不同密度接种到 96 孔板中。孵育过夜后,用无血清培养基替换细胞,然后用测定缓冲液(自发 LDH 释放)或 10% Triton X-100 溶液(最大 LDH 释放)处理。处理后,除去培养基并放入新的 96 孔板中。使用 LDH Cytotoxicity Assay Kit #37291 实验步骤确定释放到培养基中的 LDH 量。
通过流式细胞术进行免疫表型分析
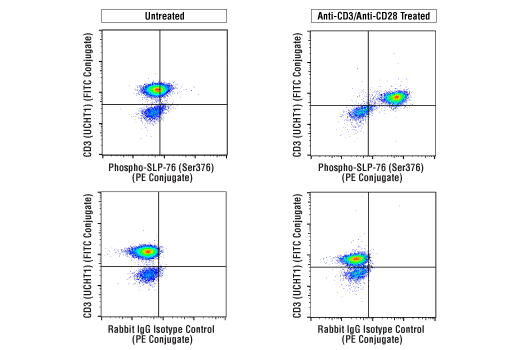
使用 Phospho-SLP-76 (Ser376) (E3G9U) XP® Rabbit mAb (PE Conjugate) #76143(上行)或浓度匹配的 Rabbit (DA1E) mAb IgG XP® Isotype Control (PE Conjugate) #5742(下行)和共染色的 CD3 (UCHT1) Mouse mAb (FITC Conjugate) #86774 对未经处理(左栏)或已经过交联抗 CD3 + 抗 CD28(各 10 μg/ml,15 分钟;右栏)处理的人外周血单核细胞进行流式细胞分析。
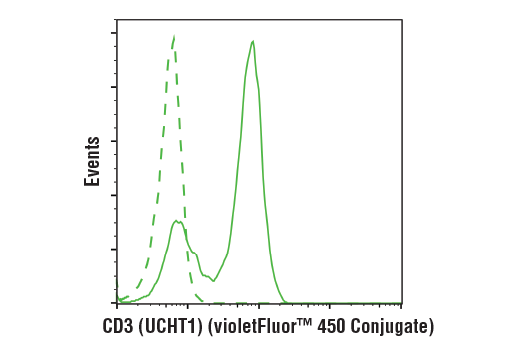
与浓度匹配的 Mouse (MOPC-21) mAb IgG1 Isotype Control (violetFluor 450 Conjugate) #40282(虚线)比较,使用 CD3 (UCHT1) Mouse mAb (violetFluor 450 Conjugate) #61347(实线)对活性人外周血单核细胞进行流式细胞分析。
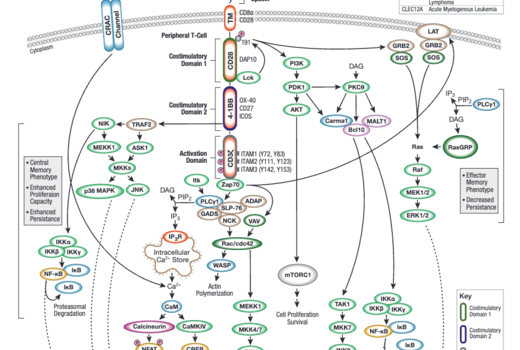
CAR-T 细胞激活的下游信号转导解析
检测 CAR 分子的细胞表面表达
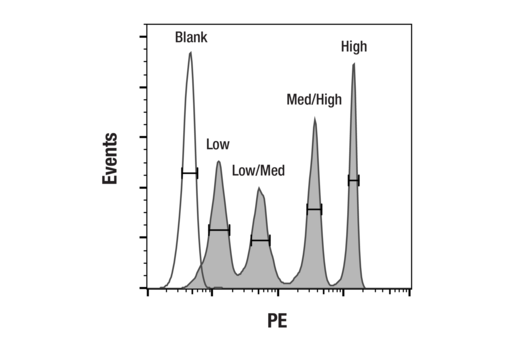
流式细胞术代表性直方图叠加展示 PE 标记珠子(阴影峰)与空白珠子(无阴影峰)的四种荧光强度。
监测 CAR 转导效率
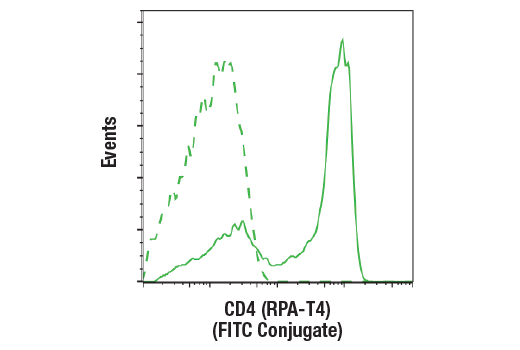
以浓度匹配的 Mouse (MOPC-21) mAb IgG1 Isotype Control (FITC Conjugate) #97146(虚线)作为对照,使用 CD4 (RPA-T4) Mouse mAb (FITC Conjugate)(实线)对活的人外周血单核细胞进行流式细胞分析。
基于微珠的 CAR+ 细胞分选
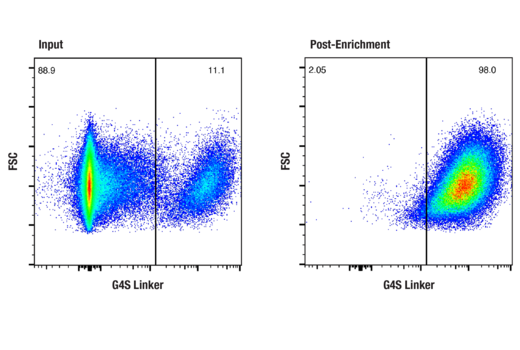
使用生物素化的 G4S Linker (E7O2V) Rabbit mAb 对输入(左图)和富集后(右图)中的活性细胞进行流式细胞分析,以进行富集。输入由 CD4+/CD8+ 人 T 细胞组成,其中包含未转导细胞的混合物和用含有 G4S Linker 的基于 scFv 的抗 CD20(Leu16)CAR 转导的细胞。富集后样本显示在细胞表面表达 CAR 的细胞群几乎纯净。Anti-rabbit IgG (H+L), F(ab')2 Fragment (Alexa Fluor® 647 Conjugate) #4414 用作二抗,以检测生物素化抗体。
基于 FACS 的 CAR+ 细胞分选
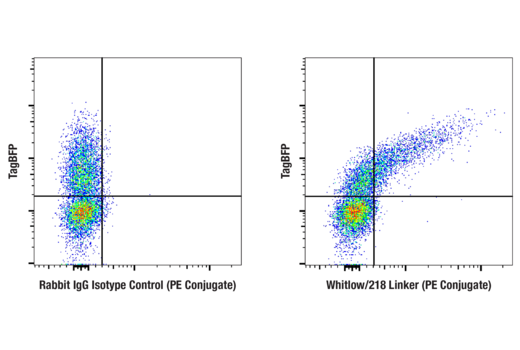
使用 Whitlow/218 Linker (E3U7Q) Rabbit mAb (PE Conjugate) #62405(右图)或浓度匹配的 Rabbit (DA1E) mAb IgG XP® Isotype Control (PE Conjugate) #5742(左图),对活性泛 CD3+ T 细胞进行流式细胞分析,这类细胞分离自人 PBMC 并经工程化以表达含有 Whitlow/218 Linker 的基于 scFv 的抗 CD19 CAR。标签蓝色荧光蛋白 (TagBFP) 与 CAR 共表达。数据由 Lohmueller 实验室(匹兹堡大学)的 Michael Kvorjak 提供。
用于转化研究的工具
当用 CAR 工程化细胞攻击实体瘤时,一个关键问题是这些细胞能否进入肿瘤微环境。传统方法存在显著局限性。值得庆幸的是,现在可以使用市售抗体直接检测实体瘤中 CAR 蛋白的表达。
研究组织中的 CAR 表达
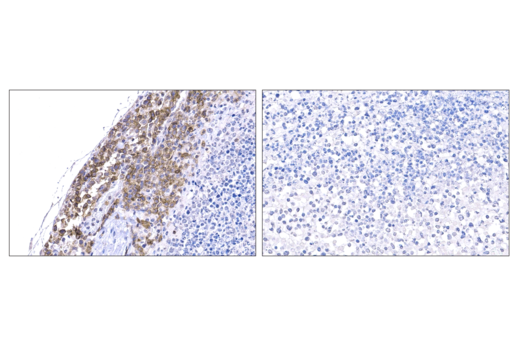
使用 Whitlow/218 Linker (F2G3S) Rabbit mAb #47414 对输注了原代人抗 CD19 CAR-T 细胞(左)或 PBS 对照(右)的 NSG 小鼠脾脏中的 Raji B 细胞淋巴瘤异种移植物进行免疫组织化学分析。
探究肿瘤微环境
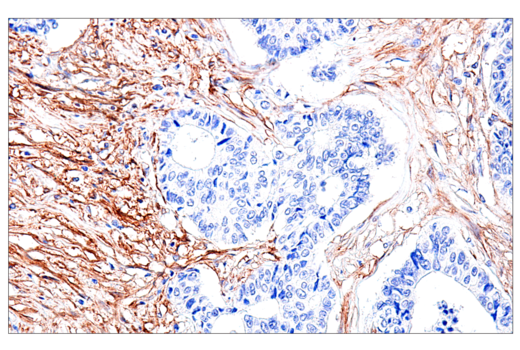
使用 FAP (F1A4G) Rabbit mAb #52818 对石蜡包埋的人结肠癌组织进行免疫组织化学分析。
CAR-工程化细胞检测资源
探索不断丰富的网络研讨会、科学海报、应用说明和其他专注于 CAR 细胞检测的资源库。
网络研讨会和视频
了解 CAR Linker 抗体如何探究不同 CAR 的表达。
评估 CAR-T 细胞信号转导和激活的分析工具 (45:23)
了解使用 Bio-Techne 分析仪器和 CST 的抗 CAR Linker 抗体生成 CD19 CAR-T 细胞的简化工作流程。
CST 的创新性单克隆Linker抗体无需为开发的每种新嵌合抗原受体 (CAR) 分子研发独特的检测试剂,从而加快流式细胞术检验组合检测。
常见问题
G4S Linker (E7O2V) Rabbit mAb 是否可以检测具有单个 G4S 重复序列的基于 scFv 的 CAR? | 不可以,E7O2V 与基于 scFv 的 CAR 最佳结合需要两次或更多次 G4S 序列重复。 |
是否知道 G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 的 Kd? | 可以。G4S Linker (E7O2V) Rabbit mAb 的 Kd 为 ~1–2 nM,而 Whitlow/218 Linker (E3U7Q) Rabbit mAb 的 Kd 为 ~2.5 nM。 |
你们是否已测试过 G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 能否与具有不同 Ag 特异性的 scFv 结合? | 可以。我们已验证 G4S Linker (E7O2V) Rabbit mAb 可与 4 种不同的 scFv 结合,Whitlow/218 linker 可与 4 种不同的 scFv 结合。 |
你们是否已测试过 G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 能否检测 FFPE 组织中的 CAR 工程化细胞? | 可以。很遗憾,G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 都不适合检测 FFPE 组织中的 CAR 工程化细胞。但是,我们推出了已获准用于 FFPE 中的 IHC 的 Whitlow/218 Linker (F2G3S) Rabbit mAb。 |
你们是否已测试过 G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 能否用蛋白质印迹法检测细胞提取物中的 CAR? | 可以。很遗憾,G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 都不适合使用常规免疫印迹技术检测细胞提取物中的 CAR 蛋白。不过,Whitlow/218 Linker (E3U7Q) Rabbit mAb 已经过验证可在 Jess Simple Western 平台上使用,Whitlow/218 Linker (F2G3S) Rabbit mAb 已经过验证可用于蛋白质印迹分析。 |
你们是否已测试过 G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 能否使用流式细胞术检测固定细胞或固定透化细胞中的 CAR? | 可以。G4S Linker (E7O2V) Rabbit mAb 和 Whitlow/218 Linker (E3U7Q) Rabbit mAb 均可在使用活性细胞的流式细胞术检测中检测表面表达的 CAR。不建议在染色前使用固定细胞或固定透化细胞。 |
你们能提供 FDA 批准的 CAR 构建体中使用的肽接头的具体信息吗? | 可以。Yescarta、Tecartus、Breyanzi 和 Abecma 均含有 Whitlow 接头。Kymriah 包含一个 3X-G4S 接头,Carvykti 包含一个 1X-G4S 接头。 |
使用抗 G4S Linker 抗体进行基于磁珠的 CAR T 细胞纯化
CST 市售的 G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907 促进了这种新的 CAR T 细胞纯化方法的开发。作者观察到在一步法过程中 CAR T 细胞进行了高度富集,且不影响细胞活力,这表明 CST 抗体的特异性和性能使该方法取得了成功。
Harrer DC, Li SS, Kaljanac M, et al. Magnetic CAR T cell purification using an anti-G4S linker antibody. J Immunol Methods. 2024;528:113667. doi:10.1016/j.jim.2024.113667
接头特异性单克隆抗体为基于 scFv 的 CAR NK 细胞提供了一种简单可靠的检测方法
本文证明了 CST Whitlow/218 和 G4S 接头特异性单克隆抗体在检测和分析基于 scFv 的 CAR NK 细胞中的实用性。这些抗体可用于通过流式细胞术在各种实验环境中(包括体外培养、全血样本和肿瘤球体)以高特异性和灵敏度可靠地识别 CAR NK 细胞。此外,该研究还强调了抗体在功能测定和 CAR NK 细胞的正向选择中的作用,展示了它们作为推进 CAR NK 细胞研究和临床应用的多功能工具的有效性。
Schindler K, Ruppel KE, Müller C, Koehl U, Fricke S, Schmiedel D. Linker-specific monoclonal antibodies present a simple and reliable detection method for scFv-based CAR NK cells. Mol Ther Methods Clin Dev. 2024;32(3):101328. 2024 8 月 22 日. doi:10.1016/j.omtm.2024.101328
合成免疫检查点接合剂可保护 HLA 缺陷型 iPSC 及其衍生物免受先天免疫细胞毒性
本文探讨了合成免疫检查点接合剂的工程设计,以增强 HLA 缺陷型诱导多能干细胞 (iPSC) 及其衍生物的免疫逃避能力。该研究中的一个关键实验涉及使用 CST 生物素化的 G4S Linker F(ab')2 片段来评估表面表达和潜在的调节作用。抗体片段可以对表达水平和相互作用进行详细的流式细胞分析,突出了它们在优化免疫逃避策略中的实用性。
Gravina A, Tediashvili G, Zheng Y, et al. Synthetic immune checkpoint engagers protect HLA-deficient iPSCs and derivatives from innate immune cell cytotoxicity. Cell Stem Cell. 2023;30(11):1538-1548.e4. doi:10.1016/j.stem.2023.10.003
阅读更多关于 CST CAR 表征解决方案的出版物摘要
CAR 蛋白质检测工具 | 特性 |
|---|---|
G4S 单克隆抗体 |
|
Whitlow/218 单克隆抗体 |
|
Protein L |
|
表位标签抗体(Myc、FLAG 和 HA) |
|
CAR 表达的替代标记物(GFP、TagBFP、LNGGFR) |
|
抗独特型单克隆抗体 |
|
重组 CAR 靶抗原 |
|
- Mohanty R, Chowdhury CR, Arega S, Sen P, Ganguly P, Ganguly N. CAR T cell therapy: A new era for cancer treatment (Review). Oncol Rep. 2019;42(6):2183-2195. doi:10.3892/or.2019.7335
- Li JH, Chen YY. A Fresh Approach to Targeting Aging Cells: CAR-T Cells Enhance Senolytic Specificity. Cell Stem Cell. 2020;27(2):192-194. doi:10.1016/j.stem.2020.07.010
- Tenspolde M, Zimmermann K, Weber LC, et al. Regulatory T cells engineered with a novel insulin-specific chimeric antigen receptor as a candidate immunotherapy for type 1 diabetes. J Autoimmun. 2019;103:102289. doi:10.1016/j.jaut.2019.05.017
- Wang D, Starr R, Alizadeh D, Yang X, Forman SJ, Brown CE. In Vitro Tumor Cell Rechallenge For Predictive Evaluation of Chimeric Antigen Receptor T Cell Antitumor Function. J Vis Exp. 2019;(144):10.3791/59275. Published 2019 2 月 27 日. doi:10.3791/59275