| Cat. # | Size | Price | Inventory |
|---|---|---|---|
| 9145T | 20 µl | ||
| 9145S | 100 µl | ||
| 9145L | 300 µl |
| REACTIVITY | H M R Mk |
| SENSITIVITY | Endogenous |
| MW (kDa) | 79, 86 |
| Source/Isotype | Rabbit IgG |
Product Information
For optimal ChIP and ChIP-seq results, use 5 μl of antibody and 10 μg of chromatin (approximately 4 x 106 cells) per IP. This antibody has been validated using SimpleChIP® Enzymatic Chromatin IP Kits.
| Application | Dilution |
|---|---|
| Western Blotting | 1:2000 |
| Simple Western™ | 1:10 - 1:50 |
| Immunoprecipitation | 1:100 |
| IHC Leica Bond | 1:100 - 1:400 |
| Immunohistochemistry (Paraffin) | 1:100 - 1:400 |
| Immunofluorescence (Immunocytochemistry) | 1:100 - 1:200 |
| Flow Cytometry (Fixed/Permeabilized) | 1:100 - 1:400 |
| Chromatin IP | 1:100 |
| Chromatin IP-seq | 1:100 |
For western blots, incubate membrane with diluted primary antibody in 5% w/v BSA, 1X TBS, 0.1% Tween® 20 at 4°C with gentle shaking, overnight.
NOTE: Please refer to primary antibody product webpage for recommended antibody dilution.
From sample preparation to detection, the reagents you need for your Western Blot are now in one convenient kit: #12957 Western Blotting Application Solutions Kit
NOTE: Prepare solutions with reverse osmosis deionized (RODI) or equivalent grade water.
Load 20 µl onto SDS-PAGE gel (10 cm x 10 cm).
NOTE: Loading of prestained molecular weight markers (#59329, 10 µl/lane) to verify electrotransfer and biotinylated protein ladder (#7727, 10 µl/lane) to determine molecular weights are recommended.
NOTE: Volumes are for 10 cm x 10 cm (100 cm2) of membrane; for different sized membranes, adjust volumes accordingly.
* Avoid repeated exposure to skin.
posted June 2005
revised June 2020
Protocol Id: 10
This protocol is intended for immunoprecipitation of native proteins utilizing Protein A agarose beads for analysis by western immunoblot or kinase activity.
NOTE: Prepare solutions with reverse osmosis deionized (RODI) or equivalent grade water.
10X Cell Lysis Buffer: (#9803) To prepare 10 ml of 1X cell lysis buffer, add 1 ml cell lysis buffer to 9 ml dH2O, mix.
NOTE: Add 1 mM PMSF (#8553) immediately prior to use.
IMPORTANT: Appropriate isotype controls are highly recommended in order to show specific binding in your primary antibody immunoprecipitation. Use Normal Rabbit IgG #2729 for rabbit polyclonal primary antibodies, Rabbit (DA1E) mAb IgG XP® Isotype Control #3900 for rabbit monoclonal primary antibodies, Mouse (G3A1) mAb IgG1 Isotype Control #5415 for mouse monoclonal IgG1 primary antibodies, Mouse (E5Y6Q) mAb IgG2a Isotype Control #61656 for mouse monoclonal IgG2a primary antibodies, Mouse (E7Q5L) mAb IgG2b Isotype Control #53484 for mouse monoclonal IgG2b primary antibodies, and Mouse (E1D5H) mAb IgG3 Isotype Control #37988 for mouse monoclonal IgG3 primary antibodies. Isotype controls should be concentration matched and run alongside the primary antibody samples.
Proceed to one of the following specific set of steps.
NOTE: When using primary antibodies produced in rabbit to detect proteins with a molecular weight in the range of 50 kDa, we recommend using Mouse Anti-Rabbit IgG (Light-Chain Specific) (D4W3E) mAb (#45262) or Mouse Anti-Rabbit IgG (Conformation Specific) (L27A9) mAb (#3678) (or HRP conjugate #5127) as a secondary antibody to minimize interference produced by denatured rabbit heavy chain. For proteins with a molecular weight in the range of 25 kDa, Mouse Anti-Rabbit IgG (Conformation Specific) (L27A9) mAb (#3678) (or HRP conjugate #5127) is recommended to minimize interference produced by denatured mouse light chain.
When using primary antibodies produced in mouse to detect proteins with a molecular weight in the range of 50 kDa, we recommend using Rabbit Anti-Mouse IgG (Light Chain Specific) (D3V2A) mAb (HRP Conjugate) (#58802) as a secondary antibody to minimize interference produced by denatured mouse heavy chain.
posted December 2008
revised October 2021
Protocol Id: 409
NOTE: Please see product datasheet or product webpage for appropriate antibody dilution^.
| Step | Reagents | Time/Temperature | |
|---|---|---|---|
| 1 | Dewax | BOND™ Dewax Solution, 100% Alcohol, BOND™ Wash Solution | Pre-programmed Leica® BOND™ |
| 2 | Antigen Retrieval | BOND™ Epitope Retrieval ER2 Solution | 20 min., 100˚C | Protocol: HIER 20 min with ER2 |
| 3 | Peroxide Block | Refine Detection Kit Peroxide Block* | 5 min. |
| WASH | BOND™ Wash Solution | 3x 0:00 min. | |
| 4 | Protein Block (optional) | #5425 NGS or #15019 Animal-Free Blocking Solution | 20 min. |
| 5 | Primary Antibody^ | Dilute in #8112 SignalStain® Antibody Diluent | 30 min. |
| WASH | BOND™ Wash Solution | 3x 2:00 min. | |
| NA | Post Primary Mouse Linker | Refine Detection Kit Post Primary* | Not Applied |
| 6 | Secondary Detection | Refine Detection Kit Polymer* | 10 min. |
| WASH | BOND™ Wash Solution/Deionized Water | Custom (see below) | |
| 7a | Visualization | Refine Detection Kit Mixed DAB Refine* | 0:00 min. |
| 7b | Visualization | Refine Detection Kit Mixed DAB Refine* | 10 min. |
| WASH | Deionized Water | 3x 0:00 min. | |
| 8 | Counterstain | Refine Detection Kit Hematoxylin* | 5 min. |
| WASH | Deionized Water | 0:00 min. | |
| WASH | BOND™ Wash Solution | 0:00 min. | |
| WASH | Deionized Water | 0:00 min. | |
| 9 | Dehydration (Offline): | ||
| Incubate sections in 95% ethanol two times for 10 seconds each. | |||
| Repeat in 100% ethanol, incubating sections two times for 10 seconds each. | |||
| Repeat in xylene, incubating sections two times for 10 seconds each. | |||
| 10 | Mount sections with coverslips and #14177 SignalStain® Mounting Medium | ||
| Optional Custom wash: | BOND™ Wash Solution | 2:00 | |
| BOND™ Wash Solution | Dispenser Type: OPEN 0:00 | ||
| BOND™ Wash Solution | 2:00 | ||
| BOND™ Wash Solution | Dispenser Type: OPEN 0:00 | ||
| BOND™ Wash Solution | 0:00 | ||
| Deionized Water | 0:00 | ||
*Reagent included in BOND™ Polymer Refine Detection Kit (Catalog No: DS9800)
LEICA® is a registered trademark of Leica Microsystems IR GmbH.
BOND™ is a trademark of Leica Biosystems Melbourne Pty. Ltd. No affiliation or sponsorship between CST and Leica Microsystems IR GmbH or Leica Biosystems Melbourne Pty. Ltd is implied.
posted August 2018
revised September 2018
Protocol Id: 1444
NOTE: Prepare solutions with reverse osmosis deionized (RODI) or equivalent grade water.
NOTE: Do not allow slides to dry at any time during this procedure.
For EDTA: Heat slides in a microwave submersed in 1X EDTA unmasking solution until boiling is initiated; follow with 15 min at a sub-boiling temperature (95°-98°C). No cooling is necessary.
| RECOMMENDED DETECTION REAGENTS |
SignalStain® Boost IHC Detection Reagent (HRP, Rabbit) #8114 | SignalStain® Boost IHC Detection Reagent (AP, Rabbit) #18653 |
|---|---|---|
|
COMPATIBLE CHROMOGEN |
SignalStain® DAB Substrate Kit #8059 | SignalStain® Vibrant Red Alkaline Phosphatase Substrate Kit #76713 |
| SignalStain® Vivid Purple Peroxidase Substrate Kit #96632 | SignalStain® Ultra Blue Alkaline Phosphatase Substrate Kit #12824 | |
| SignalStain® Deep Black Peroxidase Substrate Kit #72986 | ||
| SignalStain® Radiant Yellow Peroxidase Substrate Kit #69644 |
NOTE: Use of detection reagents other than those specified in this protocol may require further optimization of the primary antibody to account for the different sensitivities of the detection reagents.
posted February 2010
revised June 2020
Protocol Id: 284
NOTE: Prepare solutions with reverse osmosis deionized (RODI) or equivalently purified water.
Recommended Fluorochrome-conjugated Anti-Rabbit secondary antibodies:
NOTE: Cells should be grown, treated, fixed and stained directly in multiwell plates, chamber slides or on coverslips.
NOTE: All subsequent incubations should be carried out at room temperature unless otherwise noted in a humid light-tight box or covered dish/plate to prevent drying and fluorochrome fading.
posted November 2006
revised December 2010
Protocol Id: 32
All reagents required for this protocol may be efficiently purchased together in our Intracellular Flow Cytometry Kit (Methanol) #13593, or individually using the catalog numbers listed below.
NOTE: Prepare solutions with reverse osmosis deionized (RODI) or equivalent grade water.
NOTE: When including fluorescent cellular dyes in your experiment (including viability dyes, DNA dyes, etc.), please refer to the dye product page for the recommended protocol. Visit www.cellsignal.com for a full listing of cellular dyes validated for use in flow cytometry.
NOTE: Adherent cells or tissue should be dissociated and in single-cell suspension prior to fixation.
NOTE: Optimal centrifugation conditions will vary depending upon cell type and reagent volume. Generally, 150-300g for 1-5 minutes will be sufficient to pellet the cells.
NOTE: If using whole blood, lyse red blood cells and wash by centrifugation prior to fixation.
NOTE: Antibodies targeting CD markers or other extracellular proteins may be added prior to fixation if the epitope is disrupted by formaldehyde and/or methanol. The antibodies will remain bound to the target of interest during the fixation and permeabilization process. However, note that some fluorophores (including PE and APC) are damaged by methanol and thus should not be added prior to permeabilization. Conduct a small-scale experiment if you are unsure.
NOTE: Count cells using a hemocytometer or alternative method.
posted July 2009
revised June 2020
实验步骤编号:404
针对以下产品:SimpleChIP® Plus Sonication Chromatin IP Kit #56383。
包括的试剂:
未包括的试剂:
| ! | 这就表示在实验流程中基于免疫沉淀制备物(IP 制备物)数量的容积改变是重要的一步。一份 IP 制备物是指 4 x 106 个组织培养细胞或 25 mg 离体的组织。 |
| !! | 这就表示,进行操作前稀释缓冲液是重要的一步。 |
| 安全停止 | 如果需要停止,这是实验步骤中的一个安全停止点。 |
收获组织时,去除样品中不需要的物质,如脂肪和坏死物质。组织可以立即处理和交联,或放在干冰上冷冻供后续处理。为获得最佳 ChIP 结果,每次免疫沉淀使用 25 mg 组织。应额外处理 5 mg 组织用于“分析染色质消化和浓度”,并用作输入染色质(第四部分)。不同组织类型的染色质产率不尽相同,每次免疫沉淀时,某些组织可能需要超过 25 mg。
一次染色质制备量规定为 100 至 150 mg 组织。对于某些组织类型,这种建议的组织量可能会导致低产率,但在超声处理过程中可确保高效的染色质碎裂。有关不同组织类型的预期染色质产率的更多信息,请参见附录 A。
在开始之前:
(!) 所有缓冲液体积应根据实验中染色质制备物的数量按比例添加。
为获得最佳 ChIP 结果,每次免疫沉淀使用大约 4 x 106 个细胞。对于 HCT 116 细胞,这相当于 15 cm 培养皿所含细胞(在 20 ml 生长培养基中的融合度为 90%)的 1/3。应额外处理 1 x 106 个细胞用于“分析染色质消化和浓度”,并用作输入染色质(第四部分)。
一次染色质制备量规定为 1 x 107 至 2 x 107 个细胞。对于某些细胞类型,这种建议的细胞量可能会导致低产率,但在超声处理过程中可确保高效的染色质碎裂。
在开始之前:
(!) 所有缓冲液体积应根据实验中使用的 15 cm 组织培养皿(或 20 ml 悬浮细胞)的数量按比例增加。
一次染色质制备量规定为 100-150 mg 组织或 1 x 107-2 x 107 个组织培养细胞。可以同时进行多份染色质制备,只要相应增加缓冲液用量并对 1 ml 样品进行超声处理。超声处理所使用的细胞数量和样品量对于产生合适大小的染色质片段非常关键。
在开始之前:
(!) 所有缓冲液体积应根据实验中染色质制备物的数量按比例添加。
为获得最佳 ChIP 结果,每次免疫沉淀使用大约 5-10 μg 经超声处理的交联染色质(第 四 部分中确定的量)。这应大致相当于用 25 mg 离散组织或 4x106 个组织培养细胞制备的一份 100 µl 免疫沉淀制备物。在添加抗体之前,通常将 100μl 消化的染色质稀释到 400μl 1X ChIP 缓冲液中。但如果每次免疫沉淀需要多于 100 µl 的染色质,则必须将交联染色质制备物按 1:4 的稀释比例在 1X ChIP 缓冲液中稀释。在这种情况下,无需添加 蛋白 G 磁珠,尽管延长用微珠孵育的时间比较有用。
在开始之前:
(!) 所有缓冲液的用量都应按照实验中免疫沉淀物的数量成比例的增加。
注意:对于 Cell Signaling Technology 的多数抗体,每份免疫沉淀样品使用 1-2 µg 时的效果最佳。如有多份不同浓度的样品,最好让阴性对照 Normal Rabbit IgG #2729 与最高抗体浓度相匹配。
在开始之前:
(!) 所有缓冲液的用量都应按照实验中免疫沉淀物的数量成比例的增加。
在开始之前:
建议:
| 引物长度: | 24 个核苷酸 |
| 最佳 Tm: | 60℃ |
| 最佳 GC: | 50% |
| 扩增子尺寸: | 150 至 200 bp(标准 PCR) |
| 80 至 160 bp(实时荧光定量 PCR) |
标准 PCR 方法:
| 试剂 | 1 次 PCR 反应所需体积 (18 μl) |
|---|---|
| 无核酸酶的 H2O | 12.5 μl |
| 10X PCR 缓冲液 | 2.0 μl |
| 4mM dNTP 混合物 | 1.0 μl |
| 5 μM RPL30 引物 | 2.0 μl |
| Taq DNA 聚合酶 | 0.5 μl |
实时荧光定量 PCR 方法:
| 试剂 | 1 次 PCR 反应所需体积 (18 μl) |
|---|---|
| 无核酸酶的 H2O | 6 μl |
| 5 μM RPL30 引物 | 2 μl |
| SimpleChIP® Universal qPCR Master Mix #88989 | 10 μl |
| a. | 初始变性 | 95℃ 3 分钟 |
| b. | 变性 | 95℃ 15 秒 |
| c. | 复性和延伸: | 60℃ 60 秒 |
| d. | 重复步骤 b 和 c,共循环 40 次。 |
输入百分比 = 2% x 2(C[T] 2% 输入样品 - C[T] 免疫沉淀样品)
C[T] = CT = PCR 反应的平均循环阈值
用这种试剂盒制备的免疫富集的 DNA 样品可用于 ChIP-seq 。要构建下游 NG 测序用 DNA 文库,请使用与您的下游测序平台相容的 DNA 文库制备实验步骤或试剂盒。对于 Illumina® 平台上测序,我们建议使用 DNA Library Prep Kit for Illumina® (ChIP-seq, CUT&RUN) #56795 及其相关索引引物 Multiplex Oligos for Illumina® (Single Index Primers) (ChIP-seq, CUT&RUN) #29580 或 Multiplex Oligos for Illumina® (Dual Index Primers) (ChIP-seq, CUT&RUN) #47538。
建议:
从组织样品收获交联的染色质时,组织类型之间的染色质产率可能显著不同。右表提供用 100 mg 组织与 2 x 107 个 HCT 116 细胞制备的染色质的预期产量范围,以及实验步骤第 四 部分确定的预期 DNA 浓度。为了获得最佳 ChIP 结果,我们建议使用 DNA Library Prep Kit for Illumina® (ChIP-seq, CUT&RUN) #56795 及其相关索引引物 Multiplex Oligos for Illumina® (Single Index Primers) (ChIP-seq, CUT&RUN) #29580 或 Multiplex Oligos for Illumina® (Dual Index Primers) (ChIP-seq, CUT&RUN) #47538。
| 组织/细胞 | 染色质总产率 | 预期 DNA 浓度 |
|---|---|---|
| 肝 | 每 100 mg 组织使用 50 µg | 150 µg/ml |
| 脑 | 每 100 mg 组织使用 25 µg | 50 µg/ml |
| 心脏 | 每 100 mg 组织使用 105 µg | 20 µg/ml |
| HCT 116 | 100-150 μg/2 x 107 个细胞 | 100-150 μg/ml |
转录因子和辅因子结合染色质 DNA 没有结合组蛋白紧密。因此,它们在超声处理期间容易脱离染色质。在 ChIP 实验中,延长固定时间能捕获更多转录因子和辅因子,尤其是使用组织样品时。如图 7 所示,固定时间从 10 分钟延长至 30 分钟可能会减小染色质片段(左小图),但 ChIP-qPCR 表明,这会显著增加心脏组织中辅因子 RING1B 和 SUZ12 的富集(中间小图和右小图)。
通常,对于同时使用细胞和组织样品的组蛋白修饰 ChIP,10 分钟固定即可,而转录因子和辅因子可能需要长达 30 分钟的额外固定时间,尤其是使用组织样品时。
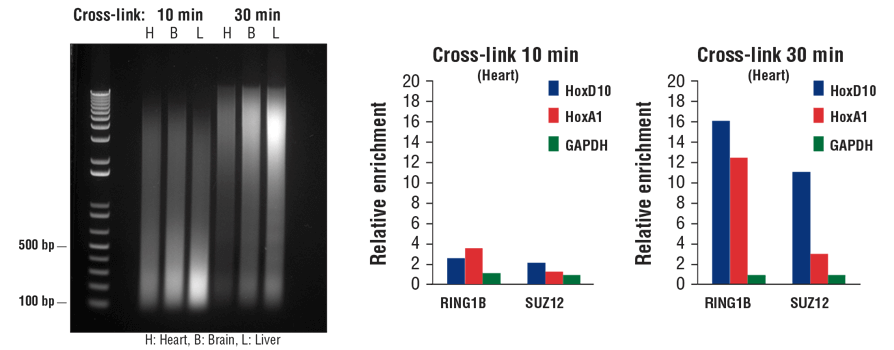
图 7. 使小鼠心脏 (H)、脑 (B) 和肝 (L) 细胞交联 10 分钟或 30 分钟,如图所示(左小图)。染色质制备后进行声处理,对 DNA 进行纯化并用 1% 琼脂糖凝胶进行电泳来分离。在 ChIP-qPCR 检测(中间和右小图)中,使用 RING1B (D22F2) XP® 兔单克隆抗体 #5694 或 SUZ12 (D39F6) XP® 兔单克隆抗体 #3737 进行染色质免疫沉淀。使用 SimpleChIP® Mouse HoxD10 Exon 1 Primers #7429、SimpleChIP® Mouse HoxA1 Promoter Primers #7341 和 SimpleChIP® Mouse GAPDH Intron 2 Primers #8986,通过实时 PCR 对富集的 DNA 进行定量分析。每份样品中免疫沉淀 DNA 的数量表示为向阴性 GAPDH 基因座发出的标准化信号(等于 1)。
交联染色质 DNA 碎裂的最佳条件高度依赖于使用的细胞数量、样品体积、超声处理时长和超声波仪功率设置。对于每份经声处理的样品,我们建议每 1 ml ChIP 声处理胞核裂解缓冲液用 100-150 mg 组织或 1 x 107-2 x 107 个细胞。 以下是确定某种特定组织或细胞类型的最佳超声处理条件的实验步骤。
注意:使用不同样品类型和固定时间时,最佳超声处理条件也不同。使用产生所需长度染色质片段需要的最少超声处理循环次数。超过 80% 短于 500 bp 的总 DNA 片段表明,过分超声处理会导致染色质过度受损,并会降低免疫沉淀效率(见图 8,右小图)
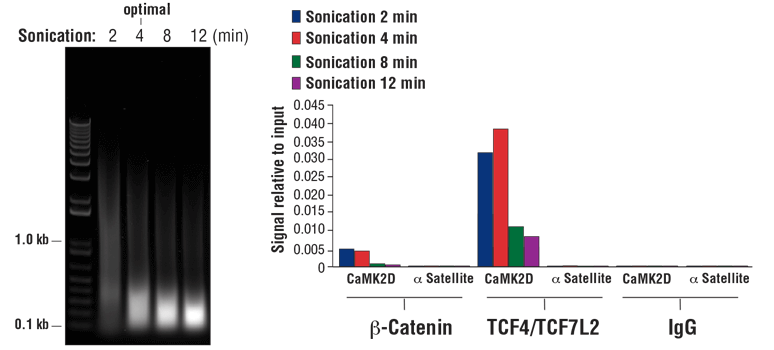
图 8. 将 HCT 116 细胞交联 10 分钟,并对其进行规定时间的声处理(左小图)。DNA 按照 SimpleChIP® Plus 超声法染色体免疫共沉淀试剂盒 #56383 的第四部分的说明进行纯化,并用 1% 琼脂糖凝胶进行电泳来分离出 20 µl 纯化的 DNA。如左小图所示,增加超声处理循环次数会减小染色质片段的大小。使用 SimpleChIP® Plus 超声法染色体免疫共沉淀试剂盒 #56383 对非磷酸化(活性)β-连环蛋白 (Ser33/37/Thr41) (D13A1) 兔单克隆抗体 #8814、TCF4/TCF7L2 (C48H11) 兔单克隆抗体 #2569 或正常兔 IgG #2729 进行染色质免疫沉淀。使用 SimpleChIP® Human CaMK2D Intron 3 Primers #5111 和 SimpleChIP® Human α Satellite Repeat Primers #4486,通过实时 PCR 对富集的 DNA 进行定量分析。每份样品中免疫沉淀的 DNA 数量表示为与输入染色质总量相对应的信号(等于 100%;右小图)。如图所示,使用配有 1/8 英寸微探头的 Branson Digital Sonifier D250 探头超声波仪时,4 分钟的染色质声处理最佳。过度超声处理会明显有损辅因子 β-catenin 和包含染色质的转录因子 TCF4/TCF7L2 的富集。
| 问题 | 可能的原因 | 建议 |
|---|---|---|
| 1. 碎裂染色质的浓度过低。 |
细胞/细胞核裂解不完全。 染色质制备没有使用足够细胞。 |
如果染色质制备物的 DNA 浓度接近于 50 μg/ml,则向每次 IP 中添加额外的染色质以确保每次 IP 至少产生 5 μg,然后继续实验。 交联前,对单独平板上的细胞进行计数,以确定准确的细胞数量。 |
| 2. 染色质碎裂不足,且片段过大(超过 50% 的片段大于 1.5 kb)。 |
细胞可能已经过度交联。 处理了过多细胞/组织。 |
将交联时间缩短到 10-30 分钟的范围。减少每次超声处理的细胞/组织数量。进行超声处理时程。 |
| 3. 染色质过度碎裂(超过 90% 的片段小于 300 bp)。 |
超声处理条件太苛刻。 |
进行一次超声处理时程来找到进行相应超声处理的最小输出/时长。 |
| 4. 样品输入对照组 PCR 反应中无产物或产物很少。 |
添加至 PCR 反应的 DNA 不足或条件不是最佳。 PCR 扩增区域可能跨越无核小体的区域。 加入到免疫沉淀的染色质不足,或染色质被过度超声处理。 |
向 PCR 反应中添加更多 DNA 或增加扩增循环次数。 使用从交联并经超声处理的染色质中获得的纯化 DNA 来优化针对实验用引物组的 PCR 条件。为获得最佳 ChIP 结果,每次 IP 添加 5-10 μg 染色质。参见上述问题 1 和 3 的建议。 |
| 5. 阳性对照组蛋白 H3-IP RPL30 PCR 反应中无产物。 |
添加至 IP 反应的染色质或抗体不足,或者 IP 孵育时间过短。 蛋白 G 微珠中染色质洗脱不完全。 |
确保每次免疫沉淀反应添加 5-10 µg 染色质和 10 µl 抗体,并用抗体孵育过夜,添加蛋白 G 微珠之后再孵育 2 小时。 在 65℃ 下将染色质从蛋白 G 微珠洗脱为最佳,同时频繁混合以保持微珠悬浮在溶液中。 |
| 6. 阴性对照 Rabbit IgG-IP 和阳性对照 Histone H3-IP PCR 反应中产物的数量相等。 |
添加至 IP 反应的染色质过多或不足。或者,添加至 IP 反应的抗体过多。 添加至 PCR 反应的 DNA 过多或扩增循环次数过多。 |
向每次 IP 反应中添加不超过 15 μg 的染色质和 10 μl Histone H3 Antibody。每次 IP 将 Normal Rabbit IgG 缩减至1 µl/IP。 向 PCR 反应中添加更少的 DNA 或减少 PCR 循环次数。在 PCR 的线性扩增阶段范围内分析 PCR 产物极为重要。否则,起始 DNA 数量的差异无法准确测量。 |
| 7. 实验抗体 IP PCR 反应中无产物。 |
添加至 PCR 反应的 DNA 不足。 添加至 IP 反应的抗体不足。 抗体不适用于 IP。 |
向 PCR 反应中添加更多 DNA 或增加扩增循环次数。 通常,免疫沉淀反应需添加 1-5 µg 抗体;但准确的用量在很大程度上取决于具体抗体。 增加添加至 IP 反应的抗体量。寻找其他替代抗体。 |
发布时间 2017 年 3 月
修订时间 2022 年 4 月
实验步骤编号:1384
针对以下产品:SimpleChIP® Plus Sonication Chromatin IP Kit #56383。
收获组织时,去除样品中不需要的物质,如脂肪和坏死物质。组织可以立即处理和交联,或放在干冰上冷冻供后续处理。为获得最佳 ChIP 结果,每次免疫沉淀使用 25 mg 组织。应额外处理 5 mg 组织用于“分析染色质消化和浓度”,并用作输入染色质(第四部分)。不同组织类型的染色质产率不尽相同,每次免疫沉淀时,某些组织可能需要超过 25 mg。
一次染色质制备量规定为 100 至 150 mg 组织。对于某些组织类型,这种建议的组织量可能会导致低产率,但在超声处理过程中可确保高效的染色质碎裂。有关不同组织类型的预期染色质产率的更多信息,请参见附录 A。
在开始之前:
为获得最佳 ChIP 结果,每次免疫沉淀使用大约 4 x 106 个细胞。对于 HCT 116 细胞,这相当于 15 cm 培养皿所含细胞(在 20 ml 生长培养基中的融合度为 90%)的 1/3。应额外处理 1 x 106 个细胞用于“分析染色质消化和浓度”,并用作输入染色质(第四部分)。
一次染色质制备量规定为 1 x 107 至 2 x 107 个细胞。对于某些细胞类型,这种建议的细胞量可能会导致低产率,但在超声处理过程中可确保高效的染色质碎裂。
在开始之前:
一次染色质制备量规定为 100-150 mg 组织或 1 x 107-2 x 107 个组织培养细胞。可以同时进行多份染色质制备,只要相应增加缓冲液用量并对 1 ml 样品进行超声处理。超声处理所使用的细胞数量和样品量对于产生合适大小的染色质片段非常关键。
在开始之前:
为获得最佳 ChIP 结果,每次免疫沉淀使用大约 5-10 μg 经超声处理的交联染色质(第 四 部分中确定的量)。这应大致相当于用 25 mg 离散组织或 4x106 个组织培养细胞制备的一份 100 µl 免疫沉淀制备物。在添加抗体之前,通常将 100μl 消化的染色质稀释到 400μl 1X ChIP 缓冲液中。但如果每次免疫沉淀需要多于 100 µl 的染色质,则必须将交联染色质制备物按 1:4 的稀释比例在 1X ChIP 缓冲液中稀释。在这种情况下,无需添加 蛋白 G 磁珠,尽管延长用微珠孵育的时间比较有用。
在开始之前:
注意:对于 Cell Signaling Technology 的多数抗体,每份免疫沉淀样品使用 1-2 µg 时的效果最佳。如有多份不同浓度的样品,最好让阴性对照 Normal Rabbit IgG #2729 与最高抗体浓度相匹配。
在开始之前:
在开始之前:
建议:
| 引物长度: | 24 个核苷酸 |
| 最佳 Tm: | 60℃ |
| 最佳 GC: | 50% |
| 扩增子尺寸: | 150 至 200 bp(标准 PCR) |
| 80 至 160 bp(实时荧光定量 PCR) |
标准 PCR 方法:
| 试剂 | 1 次 PCR 反应所需体积 (18 μl) |
|---|---|
| 无核酸酶的 H2O | 12.5 μl |
| 10X PCR 缓冲液 | 2.0 μl |
| 4mM dNTP 混合物 | 1.0 μl |
| 5 μM RPL30 引物 | 2.0 μl |
| Taq DNA 聚合酶 | 0.5 μl |
实时荧光定量 PCR 方法:
| 无核酸酶的 H2O | 6 μl |
| 5 μM RPL30 引物 | 2 μl |
| SimpleChIP® Universal qPCR Master Mix #88989 | 10 μl |
| a. | 初始变性 | 95℃ 3 分钟 |
| b. | 变性 | 95℃ 15 秒 |
| c. | 复性和延伸: | 60℃ 60 秒 |
| d. | 重复步骤 b 和 c,共循环 40 次。 |
输入百分比 = 2% x 2(C[T] 2% 输入样品 - C[T] 免疫沉淀样品)
C[T] = CT = PCR 反应的平均循环阈值
用这种试剂盒制备的免疫富集的 DNA 样品可用于 ChIP-seq 。要构建下游 NG 测序用 DNA 文库,请使用与您的下游测序平台相容的 DNA 文库制备实验步骤或试剂盒。对于 Illumina® 平台上测序,我们建议使用 DNA Library Prep Kit for Illumina® (ChIP-seq, CUT&RUN) #56795 及其相关索引引物 Multiplex Oligos for Illumina® (Single Index Primers) (ChIP-seq, CUT&RUN) #29580 或 Multiplex Oligos for Illumina® (Dual Index Primers) (ChIP-seq, CUT&RUN) #47538。
建议:
从组织样品收获交联的染色质时,组织类型之间的染色质产率可能显著不同。右表提供用 100 mg 组织与 2 x 107 个 HCT 116 细胞制备的染色质的预期产量范围,以及实验步骤第 四 部分确定的预期 DNA 浓度。为了获得最佳 ChIP 结果,我们建议使用 DNA Library Prep Kit for Illumina® (ChIP-seq, CUT&RUN) #56795 及其相关索引引物 Multiplex Oligos for Illumina® (Single Index Primers) (ChIP-seq, CUT&RUN) #29580 或 Multiplex Oligos for Illumina® (Dual Index Primers) (ChIP-seq, CUT&RUN) #47538。
| 组织/细胞 | 染色质总产率 | 预期 DNA 浓度 |
|---|---|---|
| 肝 | 每 100 mg 组织使用 50 µg | 150 µg/ml |
| 脑 | 每 100 mg 组织使用 25 µg | 50 µg/ml |
| 心脏 | 每 100 mg 组织使用 105 µg | 20 µg/ml |
| HCT 116 | 100-150 μg/2 x 107 个细胞 | 100-150 μg/ml |
转录因子和辅因子结合染色质 DNA 没有结合组蛋白紧密。因此,它们在超声处理期间容易脱离染色质。在 ChIP 实验中,延长固定时间能捕获更多转录因子和辅因子,尤其是使用组织样品时。如图 7 所示,固定时间从 10 分钟延长至 30 分钟可能会减小染色质片段(左小图),但 ChIP-qPCR 表明,这会显著增加心脏组织中辅因子 RING1B 和 SUZ12 的富集(中间小图和右小图)。
通常,对于同时使用细胞和组织样品的组蛋白修饰 ChIP,10 分钟固定即可,而转录因子和辅因子可能需要长达 30 分钟的额外固定时间,尤其是使用组织样品时。

图 7. 使小鼠心脏 (H)、脑 (B) 和肝 (L) 细胞交联 10 分钟或 30 分钟,如图所示(左小图)。染色质制备后进行超声处理,DNA 进行纯化并通过对 1% 琼脂糖凝胶进行电泳来分离 20 µl。在 ChIP-qPCR 检测(中间小图和右小图)中,使用 10 µl RING1B (D22F2) XP® Rabbit mAb #5694 或 5 µl SUZ12 (D39F6) XP® Rabbit mAb #3737 进行染色质免疫沉淀。使用 SimpleChIP® Mouse HoxD10 Exon 1 Primers #7429、SimpleChIP® Mouse HoxA1 Promoter Primers #7341 和 SimpleChIP® Mouse GAPDH Intron 2 Primers #8986,通过实时 PCR 对富集的 DNA 进行定量分析。每份样品中免疫沉淀 DNA 的数量表示为向阴性 GAPDH 基因座发出的标准化信号(等于 1)。
交联染色质 DNA 碎裂的最佳条件高度依赖于使用的细胞数量、样品体积、超声处理时长和超声波仪功率设置。对于每份声处理样品,我们建议每 1 ml ChIP Sonication Nuclear Lysis Buffer 使用 100-150 mg 组织或 1 x 107 - 2 x 107 个细胞。 以下是确定某种特定组织或细胞类型的最佳超声处理条件的实验步骤。
注意:使用不同样品类型和固定时间时,最佳超声处理条件也不同。使用产生所需长度染色质片段需要的最少超声处理循环次数。超过 80% 短于 500 bp 的总 DNA 片段表明,过分超声处理会导致染色质过度受损,并会降低免疫沉淀效率(见图 8,右小图)

图 8. 对交联 10 分钟并经超声处理规定时长的 2 x 107 个 HCT 116 细胞进行染色质免疫沉淀(左小图)。DNA 按照 SimpleChIP® Plus Sonication Chromatin IP Kit #56383 的第 四 部分的说明进行纯化,并在 1% 琼脂糖凝胶上进行电泳来分离 20 µl 纯化 DNA。如左小图所示,增加超声处理循环次数会减小染色质片段的大小。使用 SimpleChIP® Plus Sonication Chromatin IP Kit #56383 对 5 µl Non-phospho (Active) Β-Catenin (Ser33/37/Thr41) (D13A1) Rabbit mAb #8814、10 µl TCF4/TCF7L2 (C48H11) Rabbit mAb #2569 或 2 µl Normal Rabbit IgG #2729 进行染色质免疫沉淀。使用 SimpleChIP® Human CaMK2D Intron 3 Primers #5111 和 SimpleChIP® Human α Satellite Repeat Primers #4486,通过实时 PCR 对富集的 DNA 进行定量分析。每份样品中免疫沉淀 DNA 的数量表示为与输入染色质的总量(等于 1;右小图)相对应的信号。如图所示,使用配有 1/8 英寸微探头的 Branson Digital Sonifier D250 探头超声波仪时,4 分钟的染色质声处理最佳。过度超声处理会明显有损辅因子 β-catenin 和包含染色质的转录因子 TCF4/TCF7L2 的富集。
| 问题 | 可能的原因 | 建议 |
|---|---|---|
| 1. 碎裂染色质的浓度过低。 |
细胞/细胞核裂解不完全。 染色质制备没有使用足够细胞。 |
如果染色质制备物的 DNA 浓度接近于 50 μg/ml,则向每次 IP 中添加额外的染色质以确保每次 IP 至少产生 5 μg,然后继续实验。 交联前,对单独平板上的细胞进行计数,以确定准确的细胞数量。 |
| 2. 染色质碎裂不足,且片段过大(超过 50% 的片段大于 1.5 kb)。 |
细胞可能已经过度交联。 处理了过多细胞/组织。 |
将交联时间缩短到 10-30 分钟的范围。减少每次超声处理的细胞/组织数量。进行超声处理时程。 |
| 3. 染色质过度碎裂(超过 90% 的片段小于 300 bp)。 |
超声处理条件太苛刻。 |
进行一次超声处理时程来找到进行相应超声处理的最小输出/时长。 |
| 4. 样品输入对照组 PCR 反应中无产物或产物很少。 |
添加至 PCR 反应的 DNA 不足或条件不是最佳。 PCR 扩增区域可能跨越无核小体的区域。 加入到免疫沉淀的染色质不足,或染色质被过度超声处理。 |
向 PCR 反应中添加更多 DNA 或增加扩增循环次数。 使用从交联并经超声处理的染色质中获得的纯化 DNA 来优化针对实验用引物组的 PCR 条件。为获得最佳 ChIP 结果,每次 IP 添加 5-10 μg 染色质。参见上述问题 1 和 3 的建议。 |
| 5. 阳性对照组蛋白 H3-IP RPL30 PCR 反应中无产物。 |
添加至 IP 反应的染色质或抗体不足,或者 IP 孵育时间过短。 蛋白 G 微珠中染色质洗脱不完全。 |
确保每次免疫沉淀反应添加 5-10 µg 染色质和 10 µl 抗体,并用抗体孵育过夜,添加蛋白 G 微珠之后再孵育 2 小时。 在 65℃ 下将染色质从蛋白 G 微珠洗脱为最佳,同时频繁混合以保持微珠悬浮在溶液中。 |
| 6. 阴性对照 Rabbit IgG-IP 和阳性对照 Histone H3-IP PCR 反应中产物的数量相等。 |
添加至 IP 反应的染色质过多或不足。或者,添加至 IP 反应的抗体过多。 添加至 PCR 反应的 DNA 过多或扩增循环次数过多。 |
向每次 IP 反应中添加不超过 15 μg 的染色质和 10 μl Histone H3 Antibody。每次 IP 将 Normal Rabbit IgG 缩减至1 µl/IP。 向 PCR 反应中添加更少的 DNA 或减少 PCR 循环次数。在 PCR 的线性扩增阶段范围内分析 PCR 产物极为重要。否则,起始 DNA 数量的差异无法准确测量。 |
| 7. 实验抗体 IP PCR 反应中无产物。 |
添加至 PCR 反应的 DNA 不足。 添加至 IP 反应的抗体不足。 抗体不适用于 IP。 |
向 PCR 反应中添加更多 DNA 或增加扩增循环次数。 通常,免疫沉淀反应需添加 1-5 µg 抗体;但准确的用量在很大程度上取决于具体抗体。 增加添加至 IP 反应的抗体量。寻找其他替代抗体。 |
发布时间 2017 年 3 月
修订时间 2022 年 4 月
实验步骤编号:1404
人, 小鼠, 大鼠, 猴
仓鼠 , 牛 , 猪 , 马
使用与小鼠 Stat3 中 Tyr705 周围残基相对应的合成磷酸肽,对动物进行免疫接种来产生单克隆抗体。
Stat3 转录因子是众多细胞因子和生长因子受体的重要信号转导 (1),对胎鼠发育必不可少 (2)。研究显示 Stat3 在多种人类肿瘤中持续激活 (3,4) ,并有致癌的潜在可能性 (5),具有抗凋亡活性 (3)。Stat3 通过 Tyr705 位点的磷酸化而激活,从而诱导二聚化、核转位、DNA 结合 (6,7)。转录激活似乎受到 MAPK 或 mTOR 通路介导的 Ser727 位点磷酸化的调控 (8,9)。Stat3 同工型的表达反应了生物学功能,Stat3α (86 kDa) 和 Stat3β (79 kDa) 相对表达水平,依赖于细胞类型、配体暴露或者细胞发育的成熟阶段 (10) 。值得注意的是,Stat3β 蛋白在羧基末端转录激活结构域缺少丝氨酸磷酸化位点 (8)。
探索与本品相关的通路。
除非如以 CST 合法授权代表签署的书面形式另行明确同意,否则以下条款适用于 CST、其附属公司或其分销商提供的产品。除非 CST 合法授权代表以书面形式单独接受,否则任何附加于或异于此处所载条款和条件的客户条款和条件均被拒绝且无效。
产品用“仅供研究使用”或类似标示声明标示,并且尚未经 FDA 或其他国外或国内监管实体出于任何目的批准、准许或许可。客户不得出于任何诊断或治疗目的或以任何与产品标示声明相冲突的方式使用任何产品。CST 销售或许可的产品提供给作为最终用户的客户,且仅用于研究和开发用途。出于诊断、预防或治疗目的任何产品使用或出于转售(单独或作为成分)或其他商业目的的任何产品购买都要求来自 CST 的单独许可。客户 (a) 不得向任何第三方出售、许可、出借、捐赠或另行转让或提供任何本公司产品,无论单独或联合其他材料方式,或使用本公司产品制造任何商业产品,(b) 不得复制、修改、逆向工程、反编译、反汇编或另行尝试发现本公司产品的底层结构或技术,或出于开发与 CST 产品或服务竞争的任何产品或服务的目的使用本公司产品,(c) 不得从本公司产品改变或移除任何商标、商品名称、徽标、专利或版权声明或标记,(d) 仅应根据 CST 产品销售条款和任何适用文档使用本公司产品,以及 (e) 应就客户联系本公司产品所用的任何第三方产品或服务而言遵守任何许可、服务条款或类似协议。